化学ⅠB 資料4 周期表と周期律
2年 組 番 氏名( )
参考 メンデレーエフと周期表
1869 周期律を発見 約60種の元素を原子量の大きさの順に並べた。
1871 周期表を改良 空欄に入るべき未知元素の性質も予言した。
エカホウ素è( )、エカアルミニウムè( )、エカケイ素è( )
原子の構造と周期律
元素を原子番号の順に並べると、化学的性質の似た元素が周期的に現れる。
単体の融点、沸点、原子やイオンの大きさなど è 元素の(周期律)
原子番号が増すとともに、原子の価電子の数が周期的に変化することと関係している。
周期表と元素の分類
元素を原子番号の順に並べ、性質のよく似た元素が縦の欄に並ぶようにつくった表è (周期表)
(1) 周期表の横の並びを(周期)、縦の並びを(族)という。
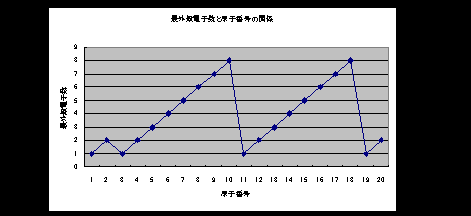
族番号の1の位の数字が最外殻電子数を示す。
(2) 同じ族の元素を(同族元素)という。
1族、2族と12~18族の元素è (典型元素)
同族元素は(価電子の数)が同じで、化学的性質が似ている。
アルカリ金属元素=1族の水素以外の元素è 1価の陽イオンになりやすい。
アルカリ土類金属元素=Be,Mg以外の2族の元素è 2価の陽イオンになりやすい。
ハロゲン=17族の元素è 1価の陰イオンになりやすい。
希ガス=18族の元素è 単原子分子で、化学的に安定。
(3) 典型元素を除く3~11族の元素è (遷移元素) 遷移金属元素
遷移元素では、族による性質の違いは典型元素ほどはっきりせず、隣り合う元素の間で性質が似ているものがある。
(4) 水素を除き、 5B 右上(非金属元素) 約20種
左下
(金属元素) 80種以上 85At
周期表と元素の性質
最外殻が同じ元素の間では、原子番号の順に
①原子半径が小さくなる
原子核の陽子の数が増え、最外殻電子が原子核の正電荷に引かれる力が強くなるため
②イオン化エネルギーが大きくなる
原子から電子をとり去って陽イオンをつくり出すのに必要なエネルギー
周期表の左側にある元素ほどイオン化エネルギーが小さく陽イオンになりやすい。
陽イオンになりやすい元素=(陽性)の元素 陰イオンになりやすい元素=(陰性)の元素
アルカリ金属 Li<Na<K<Rbの順に陽性が強くなる。
周期表の右側にいくほど、電子親和力が大きくなり、陰イオンになりやすい。
原子が電子を受け入れて陰イオンになるときに出すエネルギー
ハロゲン I<Br<Cl<Fの順に陰性が強くなる。
フッ素はすべての元素の中で最も陰性が強い。
電気陰性度=化学結合をつくるときに原子が電子を引きつける強さを表す尺度
水素と希ガスを除けば、族の番号が大きいほど、
また同族元素では周期の番号が小さいほど、è 電気陰性度は強くなる。
